NANO-Toxicología en el país de las maravillas
NANO-Toxicología en el país de las maravillas

El riesgo evoluciona: emerge, madura y muere. La fase de aparición es intensiva en la generación de conocimientos imprescindibles para la comprensión del nuevo riesgo. Hay, sin embargo, una inercia a aplicar asunciones fiables, enfoques técnicos y marcos conceptuales que funcionaron con éxito en el pasado y que son copiados ciegamente. Viejas técnicas que, hasta la fecha, habían mostrado su eficiciencia en asegurar unas mejores condiciones de vida, son las más difíciles de reemplazar, precisamente por su propio éxito. El riesgo en sí mismo es solo una expectativa, una evaluación del análisis de posibles eventos con posibles efectos adversos. (Savolainen, et al. 2014)
El reto que plantea el estudio de la toxicidad de los nanomateriales no es baladí: sencillamente los métodos de la toxicología clásica son insuficientes para afrontarlo. De momento no disponemos de un conocimiento lo suficientemente robusto - ni de caracterización de nanomateriales, ni del comportamiento de éstos una vez liberado a diferentes medios- como para establecer un modelo genérico de toxicidad. Lo que sí sabemos es que la evidencia científica disponible sobre la interacción de las nanopartículas (NP) y los nanomateriales (NM) en los sistemas vivos y en particular sobre la salud humana, es suficiente para adoptar el principio de precaución y considerarlos como potencialmente peligrosos. Ello no es óbice para comprender que esta misma evidencia es insuficiente para generar un corpus de conocimiento sobre nanotoxicología. Todavía queda mucha investigación por realizar, como pone de manifiesto las previsiones del Nanosafety Cluster de la Unión Europea, que no sitúa hasta 2025 la consecución de algunos los objetivos imprescindibles, como son la disponibilidad de métodos para la caracterización de nanomateriales complejos o la correlación entre captación, forma e impacto de los nanomateriales. A menudo ambos conceptos –la certeza sobre la toxicidad de algunos nanomateriales y la falta de herramientas para caracterizar y pronosticar su toxicidad- se confunden. Tal confusión conduce a la parálisis por análisis (Hansen, Maynard, Baun, Tickner, 2008) es decir, a no adoptar medidas de ningún tipo a la espera de tener resultados concluyentes.
Por qué es un reto
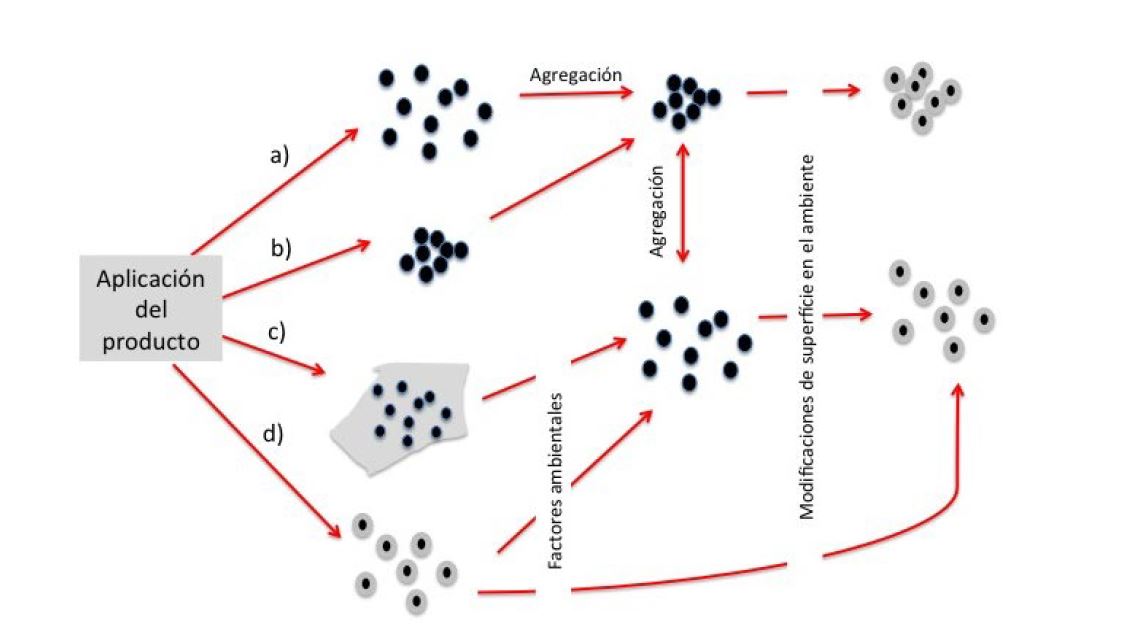
Por un lado, a la extraordinaria variabilidad de los nanomateriales, se añade el desconocimiento sobre su comportamiento una vez liberado al ambiente en forma de a) nanopartícula libre, b) nanopartículas agregadas, c) nanopartículas ligadas a una matriz o d) nanopartículas funcionalizadas; los factores ambientales, además, influyen en el grado de aglomeración y agregación (Figura 1). Por otro lado, a la inadecuación de las herramientas tradicionales y de los modelos toxicológicos disponibles, se suma la dificultad de actualización del conocimiento al ritmo que impone la aparición de nuevos productos que contienen nuevos NM. Por todo ello durante los próximos años será necesario desarrollar nuevos paradigmas de evaluación de la seguridad asociada a los nanomateriales. (Savolainen et alt, 2013).
Figura 1 Diferentes posibilidades de comportamiento de las nanopartículas una vez liberadas al medio (Nowack y Bucheli, 2007)
Para poder alcanzar una adecuada evaluación del riesgo, la investigación en nanotoxicología requiere un enfoque interdisciplinario (toxicología, ciencia de los materiales, medicina, biología molecular, bioinformática, etc.) (Oberdörster, Oberdörster,Oberdörster 2005). La investigación de las partículas ultrafinas (PUF) es el punto de partida de la nanotoxicología. Una de las hipótesis más importantes es que el peligro de las nanopartículas puede estar relacionado con propiedades fisico-químicas específicas distintas a las que se han utilizado tradicionalmente en la industria química, como por ejemplo: tamaño de partícula, forma, estructura cristalina, área superficial, química superficial y carga superficial. Ya Oberdörster et al. (1990) y Ferin et al (1990) mostraron que el dióxido de titanio ultrafino (TiO2) y el óxido de aluminio (Al2O3) de 30 nm y 20 nm, respectivamente, inducían una reacción inflamatoria muy notable en el pulmón de ratas comparada con la de las partículas de 250 nm y 500 nm. Esto es, un daño tamaño dependiente. Dos años después Oberdörster et al. (1992) informan que el estado cristalino de nanopartículas de TiO2 influye en su toxicidad y que el área superficial es mejor descriptor de los efectos adversos en ratas, que la masa. Recordemos que, a igual masa, podemos tener diferente área superficial con distinto tamaño de partícula.
La actividad biológica y la biocinética de las NP dependen de muchos parámetros, los principales a considerar para una correcta caracterización de nanopartículas en estudios toxicológicos son:
- Masa, concentración
- Composición química (pureza e impurezas)
- Solubilidad
- Área específica
- Número de partículas
- Tamaño de partícula y distribución
- Forma, porosidad
- Grado de aglomeración / agregación
- Propiedades de superficie (carga / potencial zeta, reactividad, composición química, grupos funcionales, potencial redox, potencial para generar radicales libres, presencia de metales, cobertura de superficie, etc.)
- Biopersistencia
- Estructura cristalina
- Hidrofobicidad,/hidrofilicidad
- Lugar de deposición pulmonar
- Edad de las partículas
- Productor, proceso y fuente del material utilizado
Todos estos parámetros pueden modificar las respuestas y las interacciones celulares: potencial inflamatorio, translocación a través de epitelios desde el portal de entrada hacia otros órganos, translocación por los axones y dendritas de las neuronas, inducción y estrés oxidativo, unión a proteínas y receptores, localización en la mitocondria, o actividad genotóxica y/o alteraciones epigenéticas (básicamente por metilación de histonas).
Vías de entrada en el cuerpo y mecanismos de acción de NP
Las nanopartículas pueden penetrar en el cuerpo por vía inhalatoria, por vía dérmica, por ingestión y por vía parenteral. Cuando las nanopartículas se inhalan, fracciones de determinado tamaño se depositan en el tracto respiratorio. Debido a su tamaño pueden ser captadas por las células epiteliales y endoteliales y alcanzar el torrente sanguíneo por donde son transportadas hasta órganos diana como la médula ósea, los nódulos linfáticos, el bazo o el corazón (Oberdörster et al (2007). También se ha observado el alcance del sistema nervioso central y de los ganglios por translocación a lo largo de los axones y dendritas de las neuronas. La biocinética de las nanopartículas es diferente de las partículas mayores.
En contacto con la piel, hay evidencia de penetración hasta la dermis seguida de translocación vía linfática hasta nódulos regionales linfáticos. Las nanopartículas liposolubles pueden transitar por el espacio intercelular de la capa córnea de la piel y pasar a través de las células, de los folículos capilares o de las glándulas sudoríparas (Monteiro-Riviere e Inman, 2006). Las nanopartículas pueden también almacenarse en la zona no vascularizada de la piel de donde no pueden ser eliminadas por los macrófagos. Una vez absorbidas vía dérmica también pueden alcanzar el torrente sanguíneo tras haber traspasado todas las capas de la piel.
Figura 2 Toxicocinética y lugares de acumulación de las nanopartículas (Shi et al, 2013)
Por ingestión puede darse una captación sistémica vía linfática, pero la mayoría de las nanopartículas son expulsadas vía heces. En el torrente circulatorio, pueden ser distribuidas por todo el organismo, y ser captadas a nivel de hígado, bazo, médula ósea, corazón y otros órganos. Para ciertas nanopartículas puede darse translocación desde el intestino hasta la sangre y linfa, pero depende del tamaño, carga superficial, hidrofilidad/hidrofobocidad, ligandos biológicos, recubrimientos químicos, etc. (Zhao et al,. 2007). Así, por ejemplo, la translocación sería mayor para nanopartículas hidrofóbicas y para nanopartículas pequeñas.
Una vez han penetrado en la células las nanopartículas pueden interactuar con los orgánulos celulares (mitocondrias, retículo endoplasmático rugoso, etc.) e inducen estrés oxidativo, como principal mecanismo de acción, aunque también se han descrito metilaciones de las histonas y otras alteraciones del ADN con efectos epigenéticos que tienen un papel en el desarrollo de enfermedades: cáncer (Dawson y Kouzarides, 2012; Migliore et al., 2011), enfermedades neurodegenerativas (Migliore y Coppedé, 2009), complicaciones cardiovasculares (Udali et al., 2012), alteraciones autoinmunes (Rodríguez-Cortez et al., 2011) y alteraciones de la conducta y desórdenes psiquiátricos (Miyake et al., 2012).
Recientemente Byrne, Ahluwalia, Boraschi, Fadeel y Gehr (2013) señalaban cómo las nanopartículas, en el medio biológico, pueden adquirir un recubrimiento de biomoléculas (proteínas, lípidos y polisacáridos) del entorno en el que se encuentran inmersas; tales modificaciones les confieren una identidad biológica, por lo que concluyen que, lejos de observar las nanopartículas como especies no interactivas, deben ser consideradas y estudiadas como entidades biológicas, en las que su interacción con el ambiente es mediada por proteínas y otras biomoléculas que se adsorben (en superficie) a ellas. Por ello unos parámetros clave para caracterizar a estas nanopartículas son la naturaleza, la composición y la evolución de la bio-nano interfície. Ésta es clave para comprender, además de los revestimientos de superficie, la biocinética, los fenómenos de translocación y de alteración de las señales celulares. Estamos por tanto ante un cambio de paradigma en el enfoque toxicológico tradicional, puesto que un riesgo, como es el de los nanomateriales, enfocado en principio como químico, puede adquirir una naturaleza de riesgo biológico.
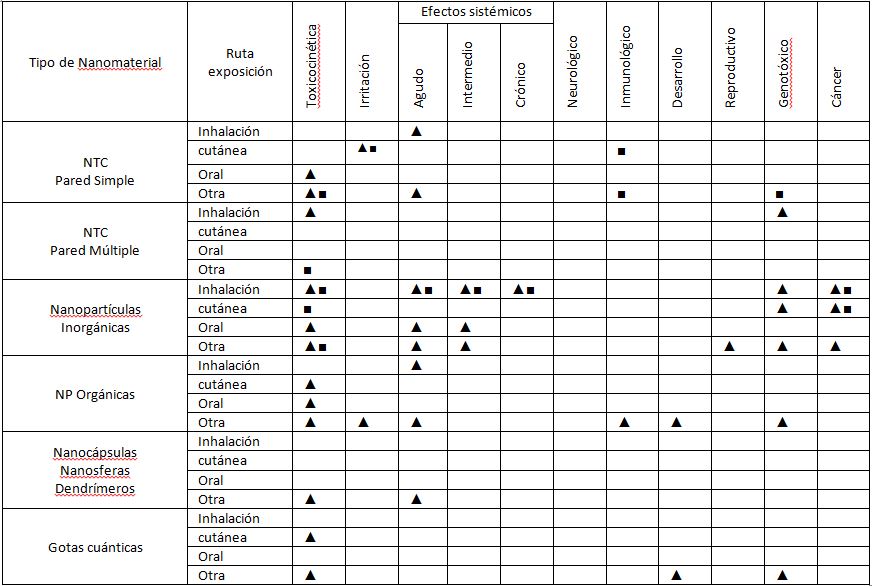
Son muchos los estudios que han proporcionado evidencias científicas sobre el impacto de determinados nanomateriales en sistemas biológicos, incluido el humano. En 2008 el IRSST publicó la segunda edición de Health effects of Nanoparticles, ordenando de forma comprensiva y en función de la ruta de exposición –inhalación, cutánea, oral y otras- la información disponible sobre toxicocinética, irritación, efectos sistémicos (agudos, intermedios y crónicos), afectación neurológica, inmunológica, del desarrollo, reproductiva, genotoxicidad y cáncer. En esta recopilación se consideraron los principales tipos de nanomateriales utilizados actualmente: nanotubos de carbono de pared simple y de pared múltiple, nanopartículas inorgánicas, nanopartículas orgánicas, nanocápsulas, nanoesferas, dendrímeros y gotas cuánticas (Tabla 1).
Tabla 1 Sumario de la toxicidad descrita entre determinados tipos de los principales nanomateriales (IRRST, 2008)
Evidencias en estudios▲(animales) y ■ (humanos)
Efectos sistémicos: agudo (< 14 días), intermedio ( 15 a 364 días) crónico (>365 días).
Consideraciones sobre el impacto de los nanomateriales en la seguridad y la salud laboral
El desarrollo de la nanotecnología ha adoptado una condición estratégica en las políticas de los países desarrollados debido a su enorme potencial y a la capacidad para abarcar problemas de calado mundial como el de la sostenibilidad, el tratamiento y detección precoz de enfermedades, la energía o la potabilización del agua. Con ello, la introducción en el mercado de productos que incorporan nanomateriales es una realidad creciente en la que participan todos los sectores de producción. Cabe preguntarse pues si ello podría afectar a la seguridad y la salud de las personas que trabajan en los centros donde se producen o manipulan productos que incorporan nanomateriales. En muchos casos el uso de este tipo de productos supone una modificación de las condiciones de trabajo, por cuanto los nanomateriales (entre 1 y 100 nanómetros) representan un riesgo diferente al del mismo material a un tamaño superior a 100 nanómetros. Ello exige legalmente una nueva evaluación de los puestos de trabajo donde se manejan tales productos. Sin embargo, como acabamos de exponer, los métodos clásicos de la toxicología son insuficientes para afrontar el reto que supone el estudio de las NP y NM que requiere de nuevos paradigmas y enfoques. ¿Qué hacer pues para garantizar la seguridad y la salud de las personas expuestas a NP y/o NM en su lugar de trabajo? La respuesta radica en dos acciones clave: de una parte, adoptar el principio de precaución y de otra, realizar una atenta vigilancia tecnológica.
Efectivamente, tras una década de trabajo en seguridad y salud ocupacional, sí que se dispone de enfoques de gestión del riesgo nano (EU-OSHA, 2013, IRSST, 2014, EU-OSHA 2014), de metodologías cualitativas -herramientas de “Control Banding” (INSHT, 2014, EU-OSHA, 2013)- para la evaluación de riesgos en nanomateriales, de medidas preventivas validadas para prevenir los riesgos laborales por exposición a NP y a NM (NIOSH, 2013), de guías dirigidas a informar a quienes trabajan en instalaciones donde se manejan o producen nanomateriales (Ponce del Castillo, 2013, EU-OSHA, 2013b, 2013c, 2014 b), o a facilitar la identificación de nanomateriales en función del tipo de sector y actividad de las empresas (INRS, 2014). Para una revisión de las guías de buenas prácticas y publicaciones imprescindibles sobre prevención de riesgos laborales y nanotecnología, puede consultarse la entrada de este blog "12 claves sobre nanotecnología y prevención de riesgos laborales".
En definitiva, el grado de conocimiento disponible a día de hoy sobre el impacto de la nanotecnología en la seguridad y salud laboral puede resumirse en tres ideas principales:
a) la primera es la necesidad de informar a empresarios y responsables de la administración de que el trabajo con nanomateriales supone una modificación de las condiciones de trabajo, por cuanto los nanomateriales (entre 1 y 100 nanómetros) pueden representar un riesgo diferente al del mismo material a un tamaño superior a 100 nanómetros
b) en segundo lugar, el paradigma tradicional de la higiene industrial necesita ser adapatado y modificado para el caso de los nanomateriales. Sin embargo, a día de hoy se puede afirmar que es posible proteger la seguridad y salud de los trabajadores expuestos a riesgos por exposición a NM, porque instituciones de referencia de todo el mundo han publicado guías de buenas prácticas y han identificado las mejores tecnologías disponibles para la gestión del riesgo nano
c) finalmente, se pone de manifiesto la necesidad de formación para actualizar las competencias de los profesionales de la prevención para garantizar la seguridad de las personas expuestas a nanomateriales en su lugar de trabajo.
____________________________________
Referencias
Este artículo es un extracto de otro de más extensión, y de la misma autoría, titulado "El impacto de la nanotecnología sobre la seguridad y la salud laboral" y publicado en la revista electrónica ORPjournal. Todas las referencias citadas están disponibles en el original:
Galera, A. (2015) El impacto de la nanotecnología sobre la seguridad y la salud laboral. ORPjournal 2:31-58